Ernte und Klärung von lentiviralen Vektoren im Labormaßstab mit Sartoclear Dynamics Lab-Filtrationssystemen

Einleitung
Mit dem Aufkommen der Gen- und genmodifizierten Zelltherapien sind Viren zu entscheidenden Werkzeugen in der Medizin geworden. Die Gentherapie besitzt ein erhebliches therapeutisches Potenzial für die Behandlung vieler erblich bedingter und erworbener Krankheiten¹; derzeit sind dreitausend klinische Studien mit viralen Vektoren registriert, von denen etwa 10 % lentivirale Vektoren verwenden². Über zweitausend einzigartige genmodifizierte Zellprodukte befinden sich in Entwicklung, und vier CAR-T-Therapien wurden bereits für onkologische Indikationen zugelassen. Die vielversprechenden Aussichten laufender klinischer Studien zur Gen- und Zelltherapie³,⁴ bedeuten, dass eine starke Nachfrage nach skalierbaren und kosteneffizienten Methoden zur Herstellung und Reinigung viraler Vektoren besteht⁵.
Lentivirale Vektoren (LV) werden typischerweise durch transiente Transfektion von HEK293T-Zellen mit mehreren Vektorplasmiden erzeugt⁶,⁷. Das Virus wird in den Überstand freigesetzt; daher müssen die Zellen aus dem Zellkulturmedium entfernt werden. Eine der Herausforderungen in der CAR-T-Forschung ist das Fehlen einer etablierten Standardmethode zur LV-Klärung. Ziel des Klärungsprozesses ist es, Hauptverunreinigungen zu beseitigen und die Trübung der Lösung zu reduzieren, wobei die Virusaktivität erhalten bleiben soll. Im Labormaßstab wird die Klärung üblicherweise durch Zentrifugation des Fermentationsmediums durchgeführt und anschließend durch Mikrofiltration des Überstands ergänzt¹,⁸,⁹. Die Vereinfachung von Ernte und Klärung durch eine einstufige Membranfiltration, die durch den Einsatz von Filterhilfsmitteln ermöglicht wird, würde die Effizienz der LV-Reinigung und der T-Zelltransduktion verbessern.
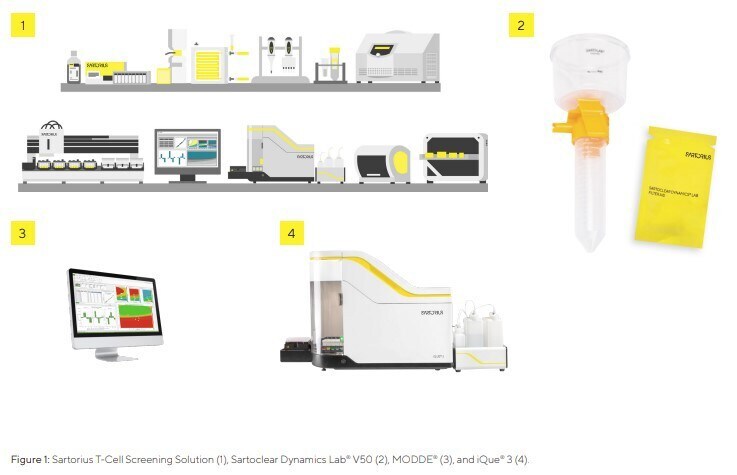
Zur Vereinfachung der CAR-T-Forschungsabläufe bietet die Sartorius T-Cell Screening Solution eine semiautomatisierte und multiplexe Methode zur Entdeckung neuer Zielstrukturen und zur Entwicklung effizienter CAR-Konstrukte (Abbildung 1). Insbesondere die Sartoclear Dynamics Lab-Produktreihe zur Klärung von Zellkulturmedien wurde entwickelt, um einen schnellen und effizienten Arbeitsablauf für die Ernte viraler Vektoren zu ermöglichen, und basiert auf dem Prinzip der dynamischen Filtration mit Filterhilfsmitteln. Das Filterhilfsmittel, Kieselgur (DE), besteht aus verschmolzenen Skelettresten von Diatomeen mit einer hochporösen Struktur¹⁰. Nach dem Upstream-Prozess wird das Kulturmedium zunächst mit dem Filterhilfsmittel vermischt und anschließend auf eine Filtermembran aufgebracht. DE bildet einen nahezu inkompressiblen porösen Filterkuchen, und seine hohe Porosität ermöglicht den Flüssigkeitsfluss um die Partikel herum, wodurch ein Verstopfen des Filters verhindert wird¹¹. Der Einsatz von Filterhilfsmitteln eliminiert den Zentrifugationsschritt und reduziert die Prozesszeit.
Material und Methoden
Der lentivirale Vektor wurde durch transiente Transfektion von HEK293T/17-SF-Zellen exprimiert, die in Suspension im UniVessel-Einwegbioreaktor mit 2 L Volumen (Sartorius) kultiviert wurden, zusammen mit vier Plasmiden, die die essenziellen lentiviralen Gene kodieren, wie ausführlich in Labisch et al.¹² beschrieben.
Die Klärung von 50 mL LV-Kulturmediumproben wurde mit der 0,45-μm-Polyethersulfon-(PES)-Version des Sartoclear Dynamics Lab V50 (Sartorius) durchgeführt. Das Sartoclear Dynamics Lab V50-Kit enthält Sartolab-RF50-Vakuumfiltrationseinheiten, die aus einem Trichter, einem 50-mL-Konusröhrchen und einem Anschlussstück für den Vakuumanschluss bestehen. Das Kit wird mit standardmäßigen Mengen von 1 g DE (Sartorius, SDLV-0050-01F0-2) oder 2 g DE (Sartorius, SDLV-0050-02F0-2) für die Filtration von bis zu 50 mL geliefert. DE-Konzentrationen von 5 g/L bis 40 g/L Kulturmedium wurden getestet. DE wurde zu 50 mL Kulturmedium gegeben, homogen vermischt und anschließend sofort filtriert. Zusätzlich wurde die Klärung von 50 mL Kulturmedium ohne DE mit einer zweistufigen Methode durchgeführt: 5-minütige Zentrifugation bei 800 × g, gefolgt von Filtration durch ein Sartolab RF50 mit einer 0,45-μm-PES-Membran (Sartorius, 180F01---------2). Zur Bestimmung der Filterkapazität wurde die Klärung bis zum Filterverschluss durchgeführt und das Filtratvolumen bestimmt. Die Vakuumfiltration erfolgte mit der Sartolab MultiStation (Sartorius, SDLC01), einem Ständer, der speziell für die Aufnahme von ein bis sechs Sartolab-RF50-Einheiten ausgelegt ist und die gleichzeitige Filtration von bis zu sechs Proben ermöglicht.
Ein Design-of-Experiment-(DOE)-Ansatz wurde verwendet, um die Klärungsbedingungen zu optimieren. Die DE-Konzentration wurde zwischen 5 g/L, 12,5 g/L und 20 g/L variiert, und die DE-Kontaktzeit zwischen 0, 10 und 20 Minuten. Die Experimente wurden als vollständiges faktorielles Design mit vier Zentrumspunkten geplant und mit der MODDE™-Software (Sartorius) ausgewertet. Analytische Parameter zur Bestimmung der Klärungsleistung waren: Trübungsbestimmung mit einem Orion™ AQUAfast AQ3010-Turbidimeter (Thermo Fisher Scientific); Gesamt-dsDNA-Konzentration (Quant-iT™ PicoGreen™, Thermo Fisher Scientific); und Gesamtproteinkonzentration (Pierce™ Coomassie Bradford Protein Assay Kit, Thermo Fisher Scientific) vor (zentrifugiertes Material) und nach der Filtration. Zusätzlich wurde der LV-Partikeltiter mittels p24-ELISA (QuickTiter™ Lentivirus Titer Kit, Cell Biolabs) bestimmt. Der Titer infektiöser lentiviraler Partikel wurde durch Transduktion adhärenter HEK293T-Zellen mit Virusproben und Messung der Transgenexpression (CD19-CAR-Konstrukt) mittels Durchflusszytometrie mit dem iQue Screener PLUS (Sartorius) bestimmt, wie zuvor beschrieben¹².
Ergebnisse und Diskussion
Bewertung des Einflusses der DE-Konzentration und der DE-Kontaktzeit auf Trübung, infektiösen Titer und Filtrationszeit in einer DOE-Studie mit MODDE
Um den Einfluss von DE auf die Klärung von LV zu untersuchen, wurden die Faktoren DE-Konzentration und Kontaktzeit für einen DOE-Ansatz ausgewählt, um deren Einfluss auf Trübung, infektiösen Titer und Filtrationszeit zu bewerten. Die Gesamtzelldichte des Kulturmediums für die DOE-Filtrationsläufe betrug 3,7 × 10⁶ Zellen/mL bei einer Trübung von 382 NTU.
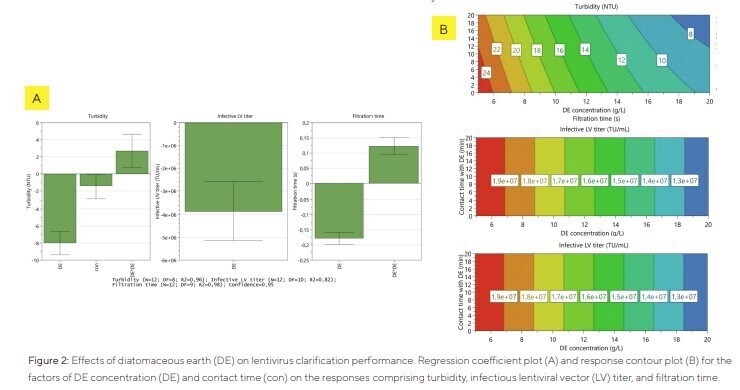
Abbildung 2 zeigt, dass infektiöser Titer und Filtrationszeit ausschließlich durch die DE-Konzentration beeinflusst werden. Mit steigender DE-Konzentration nimmt der infektiöse Titer linear ab. Für die Filtrationszeit existiert ein quadratischer Term, der zu kürzeren Filtrationszeiten innerhalb des getesteten Konzentrationsbereichs führt. Die Trübung nahm linear ab, je länger die Kontaktzeit mit DE war. Zudem verringerte eine höhere DE-Konzentration die Trübung, wobei dieser Faktor den stärksten Effekt zeigte.
Bewertung des Einflusses des Sartoclear Dynamics Lab V50 auf die Prozesszeit
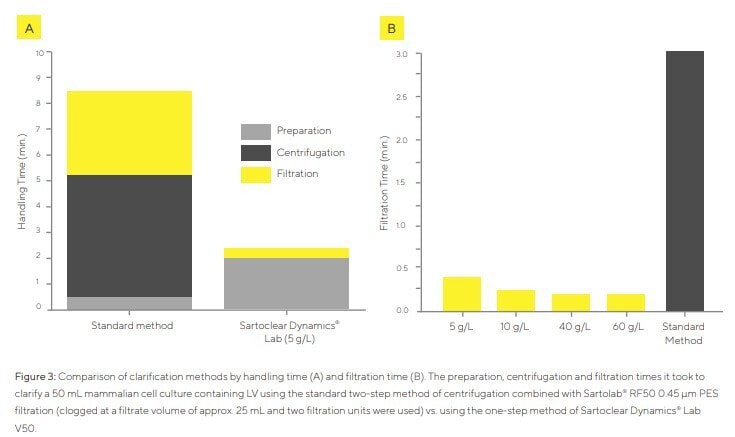
Die Handhabung des Sartoclear Dynamics Lab V50 mit verschiedenen DE-Konzentrationen wurde mit der Mikrofiltration des zentrifugierten Überstands mittels Sartolab RF50 (Standardmethode) verglichen. Nach der Ernte betrug die Zelldichte 1,11 × 10⁶ Zellen/mL und die Trübung 141 NTU. Die Gesamtprozesszeit wurde unterteilt in Vorbereitungszeit (Volumenmessung, Entfernen des Überstands, Wiegen und Zugeben von DE), Zentrifugationszeit und Filtrationszeit.
Beim Klären des zentrifugierten Überstands verstopfte der erste Sartolab-RF50-Filter nach etwa 25 mL, sodass ein zweiter Filter benötigt wurde, was die Handhabung erschwerte. Mit Sartoclear Dynamics Lab V50 verkürzte sich die Vorbereitungszeit, da der Zentrifugationsschritt entfällt (Abbildung 3A). Die Handhabungszeit wurde im Vergleich zur Standardmethode um den Faktor 3,8 reduziert. Die Filtrationszeit hing von der DE-Konzentration ab: 25 s bei 5 g/L und bis zu 13 s bei 60 g/L (Abbildung 3B).
Bewertung des Einflusses des Sartoclear Dynamics Lab V50 auf Trübung und Filterkapazität
Die Klärung wurde entweder mit Sartoclear Dynamics Lab V50 und 5 g/L DE oder mit der herkömmlichen zweistufigen Methode durchgeführt. Das verwendete Kulturmedium hatte eine Zelldichte von 3,7 × 10⁶ Zellen/mL und eine Trübung von 398 NTU.
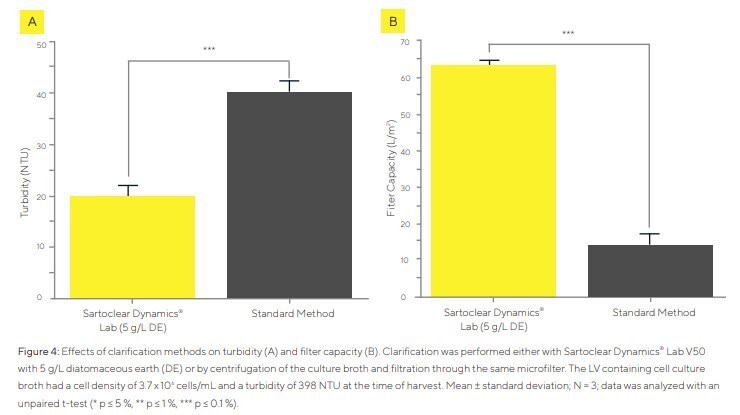
Nach Abbildung 4A führt die herkömmliche Methode zu einer Trübung von 43 NTU (89 % Reduktion), während Sartoclear Dynamics Lab V50 die Trübung um 95 % auf 21 NTU senkt. Die Filterkapazität wurde mit 5 g/L DE bestimmt. Die Filtration wurde bis zum Filterverschluss fortgeführt. Die konventionelle Methode verursachte ein schnelles Verstopfen bereits nach 33 mL. Mit 5 g/L DE wurde das maximale filtrierbare Volumen mehr als verdoppelt. Die Filterkapazität stieg deutlich (Abbildung 4B): 15 L/m² mit der Standardmethode versus etwa 63 L/m² mit 5 g/L DE. Nach Klärung mit DE lag der infektiöse LV-Titer typischerweise bei ≥ 75 % im Vergleich zu zentrifugiertem Material.
Bewertung des Einflusses des Sartoclear Dynamics Lab V50 auf die Entfernung von Verunreinigungen
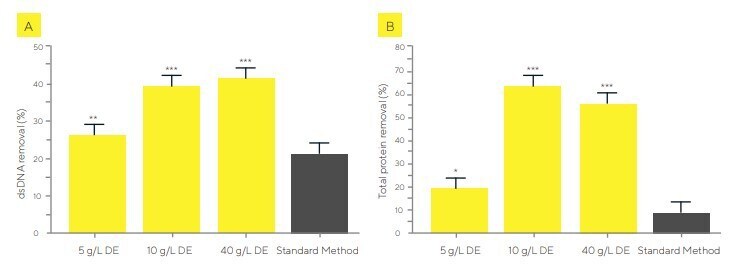
In einem separaten Experiment wurde das Potenzial des Sartoclear Dynamics Lab V50 zur Entfernung prozessbedingter Verunreinigungen durch Quantifizierung der Gesamtentfernung von Proteinen und doppelsträngiger DNA (dsDNA) untersucht (Abbildung 5).
Eine DE-Konzentration von bis zu 10 g/L erhöhte die Entfernung von Proteinen und dsDNA, aber höhere Konzentrationen zwischen 10 g/L und 40 g/L führten zu keiner weiteren Verbesserung der Reinigungsleistung. Im Gegensatz dazu zeigte der Einsatz des Sartoclear Dynamics Lab V50 eine deutlich höhere Entfernung von Verunreinigungen im Vergleich zur herkömmlichen zweistufigen Methode aus Zentrifugation und Filtration.
Fazit
Die Filtrationssysteme Sartoclear Dynamics Lab ermöglichen die Klärung von LV-haltigen Säugetierzellkulturen ohne den Einsatz einer Zentrifugation. Im Vergleich zur Standardmethode zeigte das Sartoclear Dynamics Lab V50 eine bessere Trübungsreduktion, eine stärkere Entfernung von Verunreinigungen und eine höhere Membrankapazität. Dies unterstreicht die Eignung der Sartoclear Dynamics™ Lab-Filtrationssysteme für die Ernte und Klärung lentiviraler Vektoren. Die DE-Konzentration muss jedoch angepasst werden, um hohe LV-Ausbeuten zu gewährleisten und Ertragsverluste durch eine unangemessen hohe DE-Menge zu vermeiden. Das Sartoclear Dynamics Lab V50-Kit mit DE ermöglicht eine einstufige Klärfiltration, die nicht nur eine schnellere und sicherere Handhabung erlaubt, sondern auch den Verbrauch von Labormaterialien reduziert. Das Kit ermöglicht die Auswahl einer optimalen DE-Menge, die die Filterkapazität erheblich steigert und so einen effizienten und robusten Klärungsprozess für Lentiviren in der Gen- und genmodifizierten Zelltherapie sicherstellt.
Referenzen
1 Segura, M. M., Kamen, A. A., and Garnier, A. 2011. Overview of current scalable methods for purification of viral vectors. Methods Mol Biol 737, 89–116.
2 John Wiley & Sons, Inc. 2019. Gene therapy trials worldwide. John Wiley & Sons, Inc, Hoboken, NJ, USA. J Mark Access Health Policy. Accessed 5 May 2020.
3 Hanna, E., Rémuzat, C., Auquier, P., et al. 2017. Gene therapies development: slow progress and promising prospect. Journal of market access & health policy 5, 1, 1265293.
4 Herzog, R. W., Cao, O., and Srivastava, A. 2010. Two decades of clinical gene therapy--success is finally mounting. Discov Med 9, 45, 105–111.
5 Ruscic, J., Perry, C., Mukhopadhyay, T., et al. 2019. Lentiviral Vector Purification Using Nanofiber Ion-Exchange Chromatography. Molecular therapy. Mol Ther Methods Clin Dev 15, 52–62.
6 Merten, O.-W., Schweizer, M., Chahal, P., et al. 2014. Manufacturing of viral vectors: part II. Downstream processing and safety aspects. Pharmaceutical Bioprocessing 2, 3, 237–251.
7 Sakuma, T., Barry, M. A., and Ikeda, Y. 2012. Lentiviral vectors: basic to translational. Biochem J 443, 3, 603–618.
8 Bauler, M., Roberts, J. K., Wu, C.-C., et al. 2020. Production of Lentiviral Vectors Using Suspension Cells Grown in Serum-free Media. Mol Ther Methods Clin Dev 17, 58–68.
9 Rodrigues, T., Carrondo, M. J. T., Alves, P. M., et al. 2007. Purification of retroviral vectors for clinical application: biological implications and technological challenges. J Biotechnol 127, 3, 520–541.
10 Bakr, H. E. G. M. 2010. Diatomite: Its Characterization, Modifications and Applications. Asian J Mater Sci 2, 3, 121–136.
11 Grauf, M., Lagrange, B., and Schöne, K. 2018. Simplified Small-Scale Harvest of CHO Cells for mAb Analytics. Genetic Engineering & Biotechnology News 38, 5, 22– 23.
12 Labisch, J. J., Bollmann, F., Wolff, M. W., et al. 2021. A new simplified clarification approach for lentiviral vectors using diatomaceous earth improves throughput and safe handling. J Biotechnol, 326, 11–20.
Abkürzungen
CAR - Chimärer Antigenrezeptor
(ds)DNA - (Doppelsträngige) Desoxyribonukleinsäure
DE - Diatomeenerde
DOE - Versuchsplanung / Design of Experiment
HEK - Humane embryonale Nierenzellen
LV - Lentiviraler Vektor
PES - Polyethersulfon
TU - Transduktionseinheiten
VP - Virale Partikel